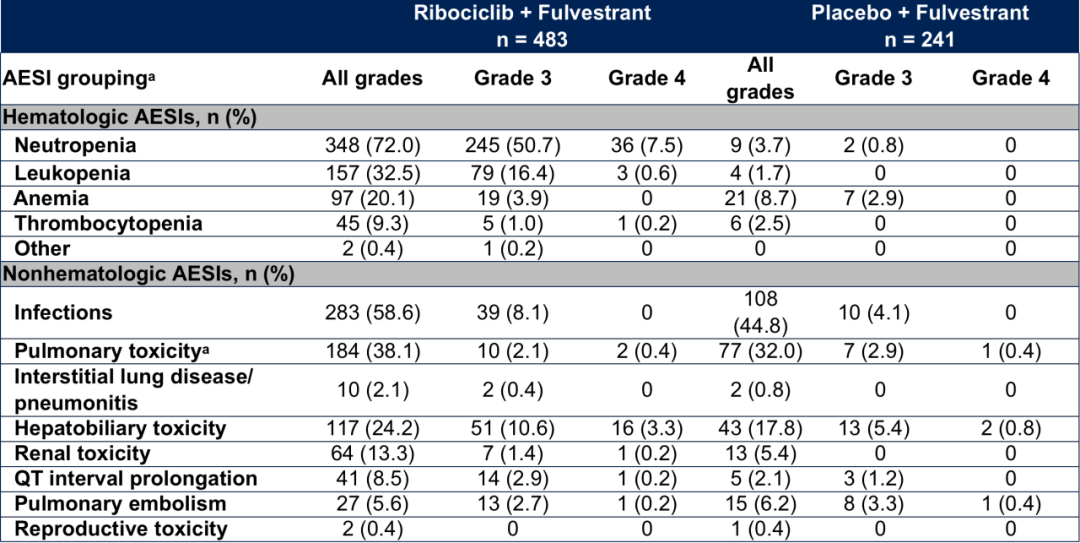
2022年欧洲肿瘤内科学会亚洲大会(ESMO ASIA)于12月2日至4日在新加坡举行,在本次大会上,来自复旦大学附属肿瘤医院的邵志敏教授代表研究团队以简短口头报告(mini oral)的形式公布了一项Ribociclib Ⅱ期桥接试验[1],为中国HR +/HER2-绝经前和绝经后晚期乳腺癌患者提供了切实的临床获益证据。 国际多中心双盲安慰剂随机对照III期MONALEESA-7(绝经前)和MONALEESA-2(绝经后)研究结果提示,与内分泌治疗(ET)相比,Ribociclib + ET初始治疗HR +/HER2-晚期乳腺癌(ABC)患者的 PFS 和 OS 具有统计学的显著获益[2,3],并且在亚洲患者亚组中观察到与意向治疗人群(ITT人群)相似的趋势。 那么上述研究结果是否适用于中国人群?为此,诺华在中国大陆HR +/HER2–绝经前和绝经后的晚期乳腺癌患者中开展了初始内分泌治疗±Ribociclib的临床研究,即Ribociclib Ⅱ期桥接试验,邵志敏教授为该研究的主要研究者(Leading PI)。研究主要分为两个队列:绝经前患者(n=156)和绝经后患者(n=154)。主要终点为研究者根据RECIST 1.1评估的无进展生存期(PFS),次要终点为总生存期(OS)、客观缓解率(ORR)和安全性。 研究结果显示,无论患者绝经状态如何,与安慰剂 + 内分泌治疗相比,Ribociclib + 内分泌治疗均显示PFS获益, 在可测量病灶人群中, 绝经前队列:Ribociclib+NSAI+OFS组较安慰剂组的ORR率有所提升(53.6% vs. 38.5%)。 绝经后队列:Ribociclib+来曲唑组较安慰剂组的ORR率也有所提升(60.3% vs. 49.3%)。 该桥接研究中Ribociclib 的总体安全性特征与Ribociclib 的已知不良反应相似,与全球研究(MONALEESA-2,7)保持一致。研究显示出Ribociclib令人鼓舞的疗效结局和良好的安全性特征,其主要分析结果补充了全球关键 MONALEESA 研究报告的结果,并为其与 内分泌治疗联合用于中国HR +/HER2−晚期乳腺癌患者提供了确切的临床获益证据。 该研究在借鉴MONALEESA-2和MONALEESA-7研究设计的基础上,将绝经前和绝经后患者两个队列同时纳入研究设计,充分展示出Ribociclib联合不同的内分泌治疗手段,在绝经前和绝经后患者中皆显示出优异的疗效和良好的安全性,是该研究的一大亮点。 2017 年 3 月,Ribociclib获美国食品药品监督管理局(FDA)批准上市,同年 8 月在欧盟获批。2022年9月,国家药品监督管理局药品审评中心(CDE)官网显示Ribociclib新适应症已经在华申报上市。该Ⅱ期桥接试验结果的公布,再次验证了Ribociclib在中国人群中的疗效,相信随着该药物可及性提高,能够进一步惠及更广大的中国患者。
Reference
[1] Primary results of a China bridging, phase II randomized study of initial endocrine therapy (ET) ± ribociclib (RIB) in pre- and postmenopausal Chinese women with HR+/HER2− ABC. 2022 ESMO ASIA: 21MO
[2] Lu YS, Im SA, Colleoni M, et al. Updated Overall Survival of Ribociclib Plus Endocrine Therapy vs Endocrine Therapy Alone in Pre- and Perimenopausal Patients With HR+/HER2- Advanced Breast Cancer in MONALEESA-7: A Phase III Randomized Clinical Trial. Clin Cancer Res. 2021 Dec 29:clincanres.3032.2021.
[3] Hortobagyi GN, Stemmer SM, et al. Overall Survival with Ribociclib plus Letrozole in Advanced Breast Cancer. N Engl J Med. 2022 Mar 10;386(10):942-950.